Investigadores de la Norwegian University of Science and Technology (NTNU), University of Life Sciences, y SINTEF revela que los desechos de la salmonicultura pueden actuar como reservorios de genes de resistencia a antibióticos. La investigación advierte que blindar la bioseguridad es clave para la sostenibilidad y seguridad del salmón en el futuro. TAGS: Salmonicultura. Resistencia antimicrobiana. Bioseguridad. Acuicultura. Sostenibilidad. Seguridad alimentaria. Industria pesquera. Salud pública
La resistencia a los antimicrobianos (RAM) es reconocida como una de las mayores amenazas para la salud pública global. Cada año, se estima que causa 1,27 millones de muertes en el mundo, y los sistemas de producción de alimentos —incluyendo la acuicultura del salmón— son piezas clave en esta compleja red de transmisión.
El salmón bajo la lupa
La industria del salmón, que en Noruega supera los 1,5 millones de toneladas anuales y a nivel global alcanza casi 3 millones de toneladas, es mucho menor en escala que la avícola, pero tiene un peso creciente en la seguridad alimentaria mundial. Garantizar su producción sostenible no solo implica bienestar animal y manejo sanitario, sino también el control de la diseminación de RAM.
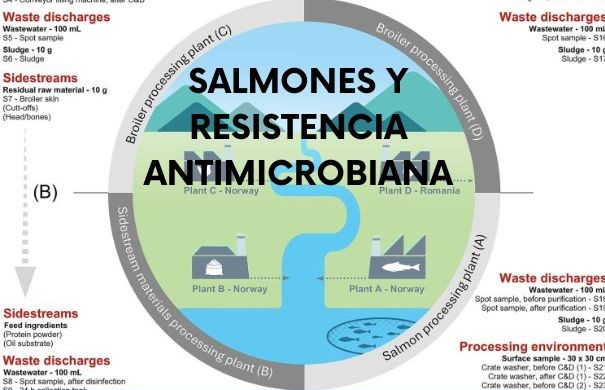
El estudio publicado en Frontiers analizó recortes de filete, intestinos y subproductos de salmón utilizados en harina de pescado y proteína en polvo. Sorprendentemente, los recortes de salmón fueron los que presentaron el mayor número de genes de resistencia a antibióticos (99 ARGs), en especial contra betalactámicos (81%), seguidos por tetraciclinas y antibióticos peptídicos. Entre ellos, destacó el gen OXA-12, previamente identificado en Aeromonas spp. asociadas a productos de sushi en Noruega.
Los investigadores sugieren que el mayor número de genes en los recortes, en comparación con los intestinos, puede deberse a contaminación cruzada durante el procesamiento y a la microbiota de la piel. Estos genes, presentes en materias primas residuales, podrían reintroducirse en nuevos sistemas de producción, especialmente en la elaboración de alimentos balanceados.
Aguas residuales: un punto crítico
En la planta de procesamiento de salmón noruega, las aguas residuales contenían 61 genes de resistencia, que se redujeron a la mitad tras el tratamiento con cloro y ajuste de pH. Aunque esta cifra es menor en comparación con las plantas avícolas (donde se detectaron hasta 330 genes), sigue siendo relevante porque las descargas de agua van directamente a los fiordos cercanos.
Entre los genes hallados en lodos y aguas residuales destacaron nuevamente los betalactámicos, además de genes asociados a resistencia frente a desinfectantes, como qacE, un hallazgo que refleja cómo los químicos de limpieza también moldean el resistoma bacteriano.
Riesgos de alto nivel
De los más de 400 genes detectados en total, 107 corresponden a genes de alto riesgo para la salud humana, capaces de transmitir resistencia a múltiples antibióticos clínicamente relevantes. Entre ellos, se encontraron genes como TolC, asociado a bombas de eflujo multidroga, y mecA, responsable de la resistencia a la meticilina en Staphylococcus aureus (MRSA).
Esto confirma que, aunque la salmonicultura noruega hace un uso muy bajo de antibióticos, los entornos industriales pueden actuar como reservorios donde la resistencia se acumula, se selecciona y, eventualmente, se libera al medio
Lo que está en juego
Los hallazgos refuerzan la necesidad de aplicar un enfoque de “Una Sola Salud” (One Health) que considere la interconexión entre humanos, animales y ambiente. En la salmonicultura, esto significa que el control de la RAM no depende únicamente de reducir el uso de antibióticos en granjas, sino también de gestionar de forma más estricta los residuos, los subproductos y las aguas de proceso.
La investigación concluye que las plantas de procesamiento de salmón, junto con las avícolas, son reservorios inadvertidos de genes resistentes. Si bien el riesgo de bacterias resistentes aisladas fue bajo, la presencia de genes en aguas, lodos y subproductos muestra que la cadena productiva puede servir de vía para su dispersión ambiental y eventual retorno al ciclo alimentario.
En definitiva, el estudio advierte que la salmonicultura, pese a su reputación de bajo uso de antibióticos, no está exenta del desafío global de la resistencia antimicrobiana. El futuro de la industria dependerá de su capacidad de blindar la bioseguridad en cada eslabón de la cadena, desde los fiordos hasta la mesa del consumidor.
Lea el estudio completo aquí: Antimicrobial resistance reservoirs in salmon and broiler processing environments, sidestreams, and waste discharges
Fuente: Infosalmon




































No hay comentarios aún.